Signale aus Zielorganen bestimmen die Differenzierung von Nervenzellen
Forschungsbericht (importiert) 2006 - Max-Planck-Institut für Hirnforschung
Entstehung unterschiedlicher Nervenzellen im autonomen Nervensystem
Die Funktion des Nervensystems basiert auf der Interaktion einer Vielzahl verschiedener Nervenzellen, die während der Entwicklung aus pluripotenten Vorläuferzellen entstehen. Das relativ einfach aufgebaute autonome Nervensystem ist ein klassisches Modell zur Analyse der Entstehung unterschiedlicher Nervenzelltypen.
Das autonome Nervensystem besteht aus sympathischen und parasympathischen Neuronen, welche die Funktionen der inneren Organe ohne bewusste Kontrolle durch das Zentralnervensystem steuern. Die wichtigsten Zielgewebe sind Herz, Blutgefäße, Lunge, Knochen, exokrine Drüsen und der Verdauungstrakt. Die verschiedenen Zielorgane werden durch funktionell unterschiedliche autonome Neuronen und übergeordente Zentren gesteuert.
Funktionelle Subtypen sympathischer Nervenzellen lassen sich aufgrund ihrer elektrophysiologischen Eigenschaften, ihrer Zielgewebe und durch die Expression von Neurotransmittern bzw. Neuropeptiden definieren. Die bislang am besten charakterisierte funktionelle Subpopulation besteht aus Nervenzellen, welche Schweißdrüsen innervieren [1, 2]. Während sympathische Nervenzellen generell Noradrenalin als synaptischen Transmitter (Überträgerstoff) einsetzen, handelt es sich bei der Schweißdrüseninnervation um so genannte cholinerge sympathische Nervenzellen, die Acetylcholin als Transmitter verwenden. Die Differenzierung dieser Zellen kann durch die Expression von charakteristischen Markergenen verfolgt werden. Interessanterweise stellte sich heraus, dass alle cholinergen Eigenschaften, wie z.B. die Expression des Acetylcholin-produzierenden Enzyms, der Cholinacetyltransferase (ChAT), des Cholin-Transporters (ChT1) und des vesikulären Acetylcholintransporters (VAChT), erst durch die Innervation des Zielgewebes induziert werden.
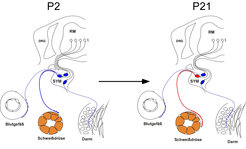
Die Schweißdrüsen werden bei Maus und Ratte in den ersten postnatalen Tagen durch noradrenerge sympathische Nervenzellaxone innerviert (Abb. 1). Im Verlauf der nächsten Wochen verlieren diese Axone ihre noradrenergen Eigenschaften und werden funktionell cholinerg. Die Entstehung funktionell verschiedener Nervenzellen in sympathischen Ganglien lässt sich also in zwei Phasen einteilen: eine frühe Phase, in der noradrenerge sympathische Neuronen entstehen, und in eine späte Phase, in der die Spezialisierung der Nervenzellen durch Signale aus den innervierten Zielgeweben gesteuert wird. In beiden Phasen spielen extrazelluläre Signale eine entscheidende Rolle. Während diejenigen Faktoren, welche die Entstehung und initiale noradrenerge Differenzierung sympathischer Neuronen induzieren, als osteogene Proteine (BMPs) charakterisiert werden konnten [3], blieb die Identität der Faktoren, welche die späte Spezialisierung bewirken, ungeklärt. Durch die selektive Eliminierung des verantwortlichen Signalwegs konnte jetzt die Identität und physiologische Relevanz dieser Signale für die cholinerge Differenzierung sympathischer Neuronen erstmals in vivo bewiesen werden [4].
Molekulare Kontrolle der frühen, noradrenergen Differenzierung sympathischer Nervenzellen
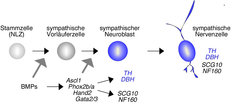
Die initiale Entstehung noradrenerger autonomer Nervenzellen wird durch osteogene Differenzierungsfaktoren (BMPs) ausgelöst, die in unmittelbarer Nachbarschaft der sympathischen Ganglienanlagen produziert werden [5]. Die BMPs induzieren in den Vorläuferzellen die Expression einer Gruppe von Transkriptionsfaktoren (Ascl1, Phox2a/b, Hand2, Gata2/3), welche direkt oder indirekt die Expression charakteristischer noradrenerger Gene, aber auch den generellen neuronalen Differenzierungsprozess steuern (Abb. 2). Essenziell für die Produktion des noradrenergen Transmitters Noradrenalin sind die Enzyme Tyrosinhydroxylase (TH) und Dopamin-β-Hydroxylase (DBH). Die Regulation der Expression ist für das DBH-Gen detailliert untersucht worden, wobei eine direkte Transkriptions-Stimulierung durch Phox2a/b und Hand2 nachgewiesen wurde. Weil eine Eliminierung des Transkriptionsfaktors Hand2 zu einem Verlust noradrenerger, nicht jedoch pan-neuronaler Eigenschaften führt, und zudem die Hand2-Überexpression eine Stimulierung noradrenerger Differenzierung bewirkt, kann gefolgert werden, dass Hand2 selektiv in die Kontrolle noradrenerger Entwicklung involviert ist [6, 7].
Molekulare Kontrolle der späten, cholinergen Differenzierung sympathischer Nervenzellen
Nachdem beobachtet worden war, dass noradrenerge sympathische Neuronen einen cholinergen Neurotransmitterphänotyp annehmen können und dass dieser Vorgang für die Entstehung der cholinergen Innervation sympathischer Zielgewebe in vivo verantwortlich ist, stellte sich die Frage nach der Identität der dafür verantwortlichen Faktoren. In vitro wurden der leukemia inhibitory factor (LIF) und die LIF-verwandten Faktoren CNTF, CT-1, OSM, CLC/CLF und Neuropoietin (CT-2) als cholinerge Differenzierungsfaktoren identifiziert [1, 2]. Sie bilden eine Familie strukturverwandter Faktoren, die auch als gp130-Zytokine bezeichnet werden. Die Bezeichnung gp130-Zytokine beruht darauf, dass alle Zellmembranrezeptoren, die diese Faktoren erkennen, gp130 als signaltransduzierende Untereinheit enthalten.
Neben den gp130-Zytokinen wurden weitere Faktoren identifiziert, die vorwiegend in vitro eine cholinerge Differenzierung in sympathischen Neuronen auslösen. Dazu zählen GDNF-verwandte Faktoren, Activin und NT-3 [8]. Da weder für die gp130-Zytokine, noch für die anderen Faktoren eine Beteiligung in der zielorganinduzierten cholinergen Differenzierung nachgewiesen werden konnte, blieb die Identität des physiologisch relevanten Faktors unklar. Eine mögliche Erklärung für fehlende Effekte des CNTF- und LIF-knockouts stellt die Kompensation durch andere Mitglieder der Familie dar. Aus diesem Grund wurde ein experimenteller Ansatz gewählt, bei dem durch Eliminierung der gp130-Rezeptor-Untereinheit die Wirkung aller Mitglieder der gp130-Zytokinfamilie verhindert werden kann. Unter Verwendung einer Mauslinie, welche die Cre-Rekombinase unter der Kontrolle der regulatorischen Regionen des DBH-Gens exprimiert, gelang es nach Kreuzung mit gp130fl/fl Tieren, gp130 selektiv in DBH-exprimierenden sympathischen Neuronen zu eliminieren [4]. Die frühe Expression von DBH führt in den gp130DBHCre Tieren bereits während der Embryonalentwicklung zum Verlust der gp130-Expression. Jetzt konnte der wichtigen Frage nachgegangen werden, welchen Effekt die Abwesenheit von gp130, mithin die Funktionsblockierung der gp130-Zytokine, in sympathischen Neuronen hat.
Die Innervation der Schweißdrüsen in gp130DBHCre Tieren weist einen fast vollständigen Verlust der Expression cholinerger Charaktere auf: Die Expression von VAChT, ChT1 und des Neuropeptids VIP, das in cholinergen Neuronen ko-exprimiert wird, ist praktisch nicht mehr nachzuweisen (Abb. 3, [4]). Die Expression pan-neuronaler Marker wie βIII-Tubulin (Tuj1, Abb. 3) und die TH-Expression (nicht gezeigt) ist dagegen unverändert. Der Verlust der cholinergen Differenzierung der Schweißdrüseninnervation spiegelt sich auch in einer starken Reduzierung der Zahl cholinerger, VIP-exprimierender Neuronen in sympathischen Ganglien wider. Dieser starke Rückgang legt nahe, dass der überwiegende Anteil cholinerger sympathischer Neuronen unter dem Einfluss von gp130-Zytokinen cholinerg differenziert.

Nachdem die Bedeutung der gp130-Zytokine durch den gp130-753 knockout gezeigt worden war, stellte sich die weiter gehende Frage, welches Mitglied aus der gp130-Familie in vivo verantwortlich ist. Dazu wurde die Expression der jeweiligen Gene in isolierten Schweißdrüsen einerseits durch Nachweis der individuellen RNAs mittels RT-PCR, anderseits durch in situ Hybridisierung untersucht. CNTF, CLC, CLF, CT-1 und NP (CT-2) wurden im Zielgewebe nachgewiesen und kommen somit als cholinerge Differenzierungsfaktoren in Frage (Abb. 4, [4]).

Der Nachweis der physiologischen Relevanz der gp130-Zytokine für die cholinerge Differenzierung sympathischer Nervenzellen bestätigt das Prinzip, dass Zielorgane die Spezialisierung von Nervenzellen steuern. Dies war auch für sensorische Nervenzellen und Motoneuronen deutlich geworden [9]. Es sollen nun die Faktoren in anderen Zielorganen, wie z.B. Blutgefäßen, identifiziert werden, welche die Differenzierung der innervierenden sympathischen Neuronen steuern.



